Wissenswertes zur Serialisierung
Ab 9. Februar 2019 dürfen in Deutschland nur noch verschreibungspflichtige Arzneimittel* in Verkehr gebracht werden, die eine packungsindividuelle Seriennummer tragen sowie einen Erstöffnungsschutz. Damit sollen Patienten vor gefälschten Arzneimitteln geschützt werden.
Die gute Nachricht für Sie zuerst ...
Es ändert sich für Sie als Arzt nichts. Die Serialisierung betrifft vor allem Hersteller und Apotheken. Allerdings sind auch Patienten betroffen, denn die Verpackung ihrer Medikamente wird sich verändern. Dies könnte auch bei Ihnen zu Rückfragen führen. Damit Sie Rückfragen schnell beantworten können finden Sie die wichtigsten Punkte im Überblick:
Stichtag ist der 9. Februar 2019. In Deutschland wurde deshalb bereits 2012 secur-Pharm e.V. gegründet, mit dem Ziel, ein nationales System aufzubauen und umzusetzen. Der Testlauf funktioniert schon seit einigen Monaten und bis zum 9. Februar 2019 wird ein System bereitgestellt, welches von allen Beteiligten am Pharmamarkt genutzt werden kann. Schrittweise werden daher bei bestehenden und neuen Produkten die Anforderungen der Gesetzgebung umgesetzt. Aus diesem Grund gibt es auch jetzt schon vereinzelt Arzneimittel mit den neuen Sicherheitsmerkmalen.
Ziel der EU-Gesetzgebung ist der Fälschungsschutz auf Packungsebene von verschreibungspflichtigen Arzneimitteln und damit der Schutz von Patienten vor Arzneimittelfälschungen. Dies soll durch den Aufbau eines europäischen Sicherungsnetzwerkes für die gesamte Lieferkette erreicht werden.
- Ein Erstöffnungsschutz oder Manipulationsschutz über den erkennbar ist, ob die Packung schon geöffnet wurde oder unversehrt ist.
- Eine individuelles Erkennungsmerkmal, das jede Packung zum Unikat und über den enthaltenen Produktcode eindeutig identifizierbar macht. Diese packungsindividuelle Seriennummer ist Basis für die Echtheitsprüfung von verschreibungspflichtigen Arzneimitteln.
So sieht der Sicherungsverschluss aus:
Zukünftig müssen verschreibungspflichtige Arzneimittel sogenannte Sicherheitsmerkmale auf Packungsebene aufweisen. Diese zwei Sicherungsmerkmale sind:
Hersteller:
Für den Hersteller bedeutet die Serialisierung eine Umstellung im Produktionsprozess. Er erzeugt die individuelle Seriennummer im Produktionsprozess und lädt sie in ein Datenbanksystem. Zudem ist er für den Öffnungsschutz verantwortlich.
Apotheke:
Die Apotheke übernimmt die Prüfung der Arzneimittel. Jede verschreibungspflichtige Arzneimittelverpackung wird bereits beim Empfang auf die Unversehrtheit des Packungssiegels geprüft und dann per Scanner über den Data-Matrix-Code in der Apotheke erfasst. Die Abgabe erfolgt nur nach positiver Prüfung.
Patienten:
Für Patienten wird vor allem die veränderte Verpackung zunächst eine Umstellung bedeuten. Insbesondere der Manipulationsschutz und dadurch umgestellte Verpackungsgrößen oder -designs könnten zu Rückfragen führen.
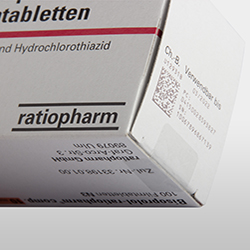
Der Code enthält verschiedene Informationen wie Produktcode, Seriennummer, Chargennummer, Haltbarkeitsdatum und evtl. nationale Kennzeichnung. Im Produktcode sind der Name des Präparates, die Darreichungsform, die Wirkstärke, die Packungsgröße und die Verpackungsart verschlüsselt.
So sieht der Code aus:

Hinweis:
*Ausnahmen siehe: DELEGIERTE VERORDNUNG (EU) 2016/161 Anhang I
Weiterführende Links zur Arzneimittelsicherheit finden Sie hier
